Le 17 mutazioni della nuova variante inglese del coronavirus

Sono ore di forte apprensione in Europa per la nuova variante di Sars-Cov-2 emersa in Inghilterra: Italia, Olanda, Germania, Francia, Belgio e Austria hanno già bloccato i voli in partenza dal Regno Unito, e altri Paesi si preparano a limitare gli arrivi da Oltremanica. Il Governo britannico ha disposto nuove più severe restrizioni in diverse aree del Paese, compresa Londra e il Sud-Est dell’Inghilterra, ovvero le regioni dove la variante mutata è diventata quella predominante: secondo quanto riportato dal ministro della Sanità britannico Matt Hancock, la variante denominata VUI-202012/01 o lignaggio B.1.1.7 è più contagiosa del 70% e in grado di aumentare l’indice Rt dello 0,4. Ma quali sono le mutazioni che conferiscono questa maggiore efficacia in termini di trasmissione?
Le mutazioni della nuova variante di Sars-Cov-2
La nuova variante – identificata per la prima volta il 20 settembre 2020 nel Kent, la contea a Sud-Est di Londra, e il 21 settembre nella Capitale – è caratterizzata da “un numero maggiore del solito di cambiamenti genetici del virus” spiegano i ricercatori del Covid-19 Genomics Consortium (CoG-UK), l’organizzazione che comprende le principali Università britanniche, nello studio in pre-print che descrive la sequenza genomica della nuova variante. Nel dettaglio, rispetto alle precedenti varianti osservate dall'inizio della pandemia (la D614G comparsa in Italia tra febbraio e marzo, la 20A.EU.1 emersa nel Nord-Est della Spagna, e il ceppo Y453 individuato in alcuni allevamenti di visoni in Danimarca) i cambiamenti nel nuovo lignaggio B.1.1.7 comprendono una combinazione unica mutazioni e delezioni specifiche, complessivamente diciassette, di cui otto interessano la proteina Spike che il virus utilizza per legare il recettore ACE2 sulle cellule umane e penetrare al loro interno.
L'elenco delle 17 mutazioni di B.1.1.7
Gene / Nucleotide / Amminoacido
ORF1ab / C3267T / T1001I
ORF1ab / C5388A / A1708D
ORF1ab / T6954C / I2230T
ORF1ab / 11288-11296 delezione / delezione SGF 3675-3677
Spike / 21765-21770 delezione / delezione HV 69-70
Spike / 21991-21993 delezione / delezione Y144
Spike / A23063T / N501Y
Spike / C23271A / A570D
Spike / C23604A / P681H
Spike / C23709T / T716I
Spike / T24506G / S982A
Spike / G24914C / D1118H
Orf8 / C27972T / Q27stop
Orf8 / G28048T / R52I
Orf8 / A28111G / Y73C
N / 28280 GAT-> CTA / D3L
N / C28977T / S235F /small>
Gli effetti già noti e quelli ancora da determinare
Come detto, buona parte delle mutazioni ricade nelle regioni dell’RNA virale che codificano per la proteina Spike e, sulla base della valutazione del loro effetto sulla struttura e funzione del virus, la più rilevante sembra essere N501Y (in arancione nella figura) che interessa residui chiave nel sito di legame per il recettore cellulare ACE2. “I dati sperimentali – indicano gli studiosi – suggeriscono che la mutazione N501Y possa aumentare l’affinità per il recettore ACE2”.
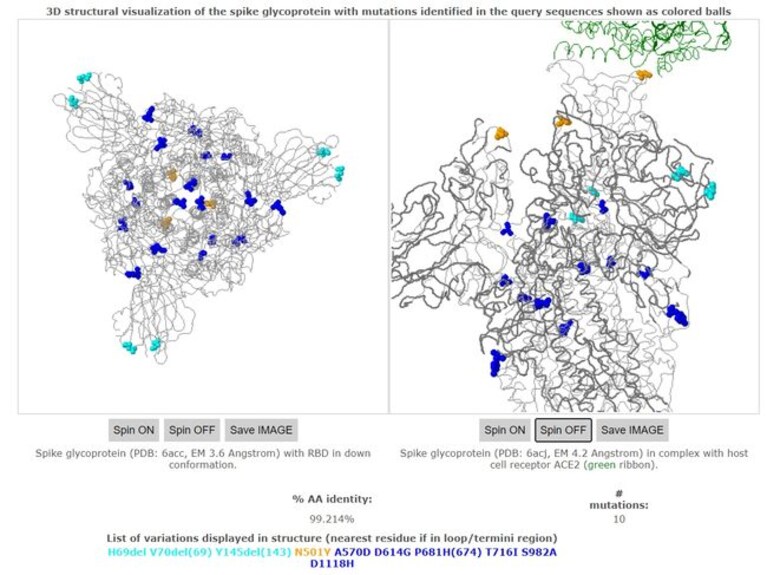
A contribuire alla potenziale variazione della superficie della proteina Spike anche le delezioni (in celeste) che interessano le regioni note per essere riconosciute da alcuni anticorpi neutralizzanti. L’effetto delle altre mutazioni (in blu), è invece meno chiaro. “La mutazione N501Y – fanno notare gli studiosi – è inoltre stata associata ad un aumento dell’infettività e della virulenza in un modello murino”. Quanto invece alla delezione di due aminoacidi nei siti 69-70, i ricercatori indicano che si tratta di uno dei cambiamenti più ricorrenti nel dominio N-terminale della proteina virale, osservato in più varianti, tra cui quella associata ai visoni in Danimarca.
Al di fuori dello Spike, la mutazione Orf8 Q27stop “tronca la proteina Orf8 o la rende inattiva, consentendo dunque l’accumulo di ulteriori mutazioni a valle”. In particolare, questa mutazione è stata osservata in altre varianti isolate, inclusa quella identificata a Singapore per cui si è scoperto che “ha solo un effetto molto modesto sulla replicazione del virus nelle cellule delle vie aeree primarie umane rispetto ai virus senza la delezione, portando a un leggero ritardo di replicazione rispetto ai virus con la delezione”. Inoltre, poiché la proteina Orf8 è solitamente formata da 121 amminoacidi, “è probabile che il codone di stop alla posizione 27 osservato nella variante B.1.1.7 provochi una perdita di funzione” e probabilmente una ridotta gravità della malattia.
Nel complesso, indicano i ricercatori, l’effetto funzionale complessivo di questa serie di mutazioni deve essere ancora determinato ma “date le conseguenze fenotipiche previste sperimentalmente e plausibili di alcune di queste mutazioni, i loro effetti sconosciuti quando presenti in combinazione e l’elevato tasso di crescita di questa nuova variante nel Regno Unito, il lignaggio B.1.1.7 richiede una caratterizzazione di laboratorio urgente e una sorveglianza genomica potenziata in tutto il mondo”.


